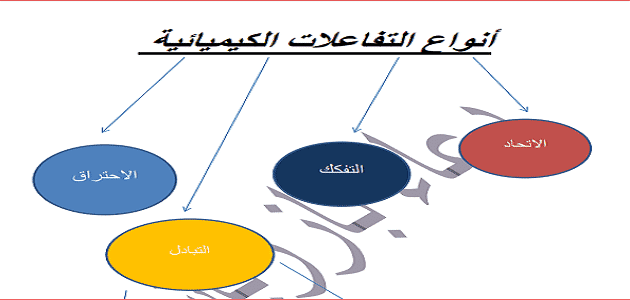
مفهوم التفاعل الكيميائى تفاعلات الإتحاد او الضم تفاعلات الإزاحه تفاعلات التحلل او التفكك التاكسد و الإختزال.
هائل من و حدات بنيوية بالغه الصغر ندعوها بالجزيئات (Molecules)، و هذة الأخيره مؤلفة من اجزاء اصغر ندعوها بالذرات (Atoms)، و التي تتفاعل مع بعضها البعض بأنواع متعددة من التفاعلات الكيميائيه و فق نظام خلقي معقد لتشكل لنا كوننا و عالمنا الواسع ذلك بأدق تفاصيله.
فما هى نوعيات التفاعلات الكيميائيه التي تحدث بين الذرات؟ و كيف تحدث و بناء علي اي اساس كيميائي؟ ذلك فالواقع ما سنستعرضة فمقالنا هذا، مستفيضين فذكر نوعيات تلك التفاعلات الكيميائيه التي تنشا بين مختلف الجزئيات و فمختلف الأوساط الفيزيائية.
التفاعلات الكيميائية
ما هى التفاعلات الكيميائية
التفاعل الكيميائى فتعريفة البسيط هو عملية تغيير كيميائيه جذريه او شبة جذريه لمركب ما بحيث ينتج علي اثر عمليه التفاعل هذة مركب احدث مختلف عن المركب الأولي الذي بدأنا به. و لب التفاعلات الكيميائيه و أساسها هو حصول تفكك فالروابط الكيميائيه المؤلفه للمركب (أو المركبات) المتفاعلة، و نشوء روابط كيميائية حديثة بين الذرات المؤلفه لتلك المركبات.
فعلي سبيل المثال و التوضيح لدينا تفاعل الاحتراق (والذى يحدث عندما تشعل نارا فبعض نوعيات غازات الأفران) كالتالي:
C3H8 + 5O2 → 4H2O + 3CO2 + energy
ما نلاحظة ان المركب الأول C3H8 كان مؤلفا من ذرتين هما الكربون C و الهيدروجين H، اما الثاني فهو جزيء الأوكسجين المؤلف من ذرتين من الأوكسجين O2. و نتيجه التفاعل الكيميائى بينهما حصلنا علي مركبين جديدين تماما، هما الماء و غاز ثاني اوكسيد الكربون.
وما حدث هنا ببساطة هو تفاعل بين مركبين حصلنا علي اثرة علي مركبين جديدين، ذلك التفاعل ندعوة بالتفاعل الكيميائي.1
سننتقل الآن الي نوعيات التفاعلات الكيميائيه المتنوعه بين المركبات المختلفه من حولنا.
أنواع التفاعلات الكيميائية
تفاعلات الأكسده –إرجاع
تتضمن عمليه الأكسده و الإرجاع تفاعلا بين مكونين احدهما نطلق علية اسم المرجع (reducing agent) اما الآخر فهو العنصر المؤكسد ( oxidizing agent). و يشتمل التفاعل علي انتقال الكترون (وهو احد المكونات الرئيسيه للذره و التي تبني علي اساسة جميع التفاعلات الكيميائية) و احد او اكثر من المرجع الي المؤكسد.
عند حدوث ذلك التفاعل بين مركبين تزداد شحنه (الشحنه الموجبه الحقيقية) للعنصر المرجع بسبب فقدانة للإلكترون السالب، فحين يكتسب العنصر المؤكسد شحنة سلبية عند التقاطة لذا الإلكترون، مشكلين بذلك عنصرا سالبا و آخر موجبا سرعان ما يتجاذبان مع بعضهما ليكونا مركبا و احدا.
وكمثال علي هذا تأكسد المغنيزيوم (Mg) و احتراقة بالأوكسجين (O2) ليشكل اوكسيد المغنيزيوم (MgO)، و ذلك المركب فيما لو حللناة فهو يتركب من Mg+2 و O-2. و أحد الأمثله الأخري الشائعه عن تفاعلات الأكسدة- ارجاع هو تشكل الصدا الذي نعرفة علي الحديد فالهواء الرطب، و صيغه التفاعل الكيميائى كالتالي:
2Fe + 2H2O + O2 → 2Fe(OH)2
فى ذلك التفاعل يحصل تأكسد للحديد لينتج عنة هيدروكسيد الحديد (الصدأ). و الجدير بالذكر ان تفاعلات الأكسدة-إرجاع هى اساس عمل البطاريات الكيميائيه التي نعتمد عليها فمختلف نواحى حياتنا، و لسنا بصدد شرح طريقة توليد الكهرباء من التفاعل الكيميائى الحاصل فيها.2
تفاعلات الاتحاد او الضم (Combination reaction)
فى تفاعلات الضم يجتمع عنصران مختلفان او اكثر متفاعلين مع بعضهما ليعطيا مركبا جديدا و احدا فقط. و تعرف ذلك النوع من التفاعلات الكيميائيه كذلك باسم التفاعلات التركيبيه (synthesis reaction)، و تأخذ الصيغه الاتيه :
X + Y → XY
وكأحد الأمثله البسيطه عن التفاعلات التركيبيه لدينا تفاعل الصوديوم Na مع الكلور Cl لتشكيل ملح الاكل الذي نعرفه، و فق الآتي:
2Na + Cl2 → 2NaCl
تفاعلات التفكك (Decomposition reaction)
وهى بالمجمل عكس التفاعلات التركيبيه التي ذكرناها سابقا، اذ تتضمن تفكك مركب مفرد الي عناصر و مركبات ابسط. و يأخذ ذلك الشكل من التفاعلات الكيميائيه الصيغه الاتية:
XY → X + Y
ويعتبر مركب حمض الكربونيك (H2CO3) مثالا حيا علي تفاعلات التفكك او التحلل، و حمض الكربونيك هو احد مكونات المشروبات الغازية، فعندما تقوم بفتح علبه المشروب تسمع خروج الهواء السريع، و ذلك ناتج عن خروج غاز ثنائى اوكسيد الكربون الناتج عن تفكك مركب حمض الكربونيك و فق المعادله الاتية:
H2CO3 → H2O + CO2
وعندما يتفكك مركب ما علي اثر تعريضة للحراره عندها نطلق علي هذا التفاعل الكيميائى مصطلح تفاعل التفكك الحرارى (thermal decomposition reaction).
تفاعلات الإزاحه او الاستبدال الأحاديه (Single displacement chemical reactions)
تشتمل هذة التفاعلات علي احد العناصر النشطه و التي تقوم بإزاحه (طرد) عنصر احدث اقل نشاط كيميائى من مركب اخر. و يأخذ ذلك التفاعل الشكل الاتي:3
A + B-C → A-C + B
والأمر المثير للاهتمام فهذا النوع من التفاعلات الكيميائيه هى ان الأسبقيه للتفاعل تكون للعناصر ذات النشاط الأكبر، فعلي سبيل المثال عند و ضع قطعة من معدن الزنك Zn فمحلول كبريتات النحاس CuSO4 ، فما نلاحظة هو ازاحه الزنك ذو النشاط الكيميائى الأكبر لعنصر النحاس من مركبة و احتلالة مكانة و فق المعادله الاتية:
Zn + CuSO4 → ZnSO4 + Cu
انواع التفاعلات الكميائية